第133回 バクテリオファージに学ぶ分子針の設計
細胞膜を貫通するタンパク質の人工分子針
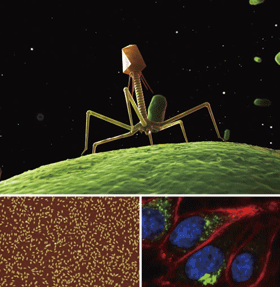
バクテリオファージT4と人工分子針
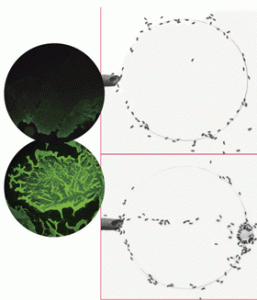
頭部に胴体、手足を備えたような形状のバクテリオファージT4は、約50種類のタンパク質からできている。天然の分子機械とも呼ばれており、尾部にあるタンパク質の針で大腸菌に孔を開けて核酸を送り込む(写真上はイメージ)。人工分子針(写真左下の電子顕微鏡写真)は幅が2.4nm、長さが16nm。右下の蛍光顕微鏡写真は、赤色が細胞膜、青が核、緑が人工分子針で、細胞に針が入っていることが確認できる。
薬を目的の細胞に届けるドラッグ・デリバリーなどへ 応用が期待される細胞内分子輸送システム。 細胞を傷つけずに自発的に細胞内に取り込まれる、 バクテリオファージに学ぶ分子針の設計とは?
細胞を保護する細胞膜は、小さな分子や疎水性の物質などを通しますが、多くの物質は透過することができません。一方、細菌に感染するバクテリオファージは、尾部にあるタンパク質の鋭い針で大腸菌の細胞に孔を開けて核酸を送り込み、大腸菌自体を殺すことなく、子孫を繁殖させています。特にT4と名付けられたバクテリオファージは、その特異的な形状と自動的に針が折れて細胞内に侵入していくメカニズムなどから、天然の分子機械とも言われています。細胞質に直接、分子を輸送するモデルとして注目され、構造解析などが盛んに行われてきました。
T4のタンパク質針は、3枚のシートがらせんを描く三重鎖βヘリックスという特徴的な構造を有していることが分かっており、その構造を人工的に再現し、細胞膜を貫通するメカニズムを明らかにしようというユニークな研究があります。すでにT4のタンパク質針を骨格とする人工分子針の合成に成功し、ほ乳類の細胞を使った実験では、蛍光色素を化学修飾した分子針が自発的に細胞膜を貫通して、細胞を破壊することなく内部に入って行くことが確認されています。
幅2.4ナノメートルという針の太さが膜の隙間にちょうど刺さると考えられますが、タンパク質針自体がなぜ自発的に入っていくのか、その詳細なメカニズムはまだわかっていません。現在、その謎を解明すべく、異なる化学修飾を施した人工分子針を使って細胞内への取り込みの比較実験などが進められています。
また、さまざまなタンパク質を人工分子針に付けた貫通実験も行われており、これまで難しいとされてきた細胞質へ直接、タンパク質を輸送する可能性も見えてきました。さらに針の先端に金属錯体を結合してカゴをつくり、近年、薬として注目されている一酸化炭素を細胞内に輸送・放出する実験にも成功しており、さまざまな物質輸送への応用が期待されているのです。
上野隆史 教授
東京工業大学 大学院生命理工学研究科

“静”のデザインから“動”のデザインへ
私は、タンパク質と金属を融合する研究を中心に行っています。いかにして機能を付加するか、そこに興味をもっています。結晶構造など、これまでは静止した状態で機能を調べて形状をデザインするという方法がとられてきました。最近では、分子が動く状態を見ることができるので、動きをうまく設計する研究が重要になってきています。
バクテリオファージT4は、さまざまな研究者によって構造解析がなされてきました。しかし構造は模倣できても、なかなか機能を付加することができていないというのが現状です。そこで、T4のタンパク質針を1つの部品としてとらえ、取り出して使ってみることで、膜貫通のメカニズムの解明に挑戦してみようと思ったのです。また、T4には他にも面白い部品構造がたくさんあります。それらをうまくデザインできれば、分子ロボットを動かすことができるかもしれません。
細胞内物質輸送には、エンドサイトーシス(細胞の飲食作用)を利用する方法があります。エンドサイトーシスは、細胞膜が通常では通さない細胞外の物質を包み込んで細胞内へ取り込む機能で、不要になったタンパク質やウイルスなどを分解除去したり、多糖類など不足物質を補充することで、細胞の代謝や生体防御などを果たすために備わっているものです。細胞膜上には、エンドサイトーシスを引き起こすためは働く受容体があり、目的に応じて取り込む物質を選択しており、エンドサイトーシスが起こる細胞にも種類があると言われています。 そのため、薬剤などを目的とする細胞内に直接輸送する方法として、生体に倣った分子針とカゴ等の容器を組み合わせた、安全で高効率な膜貫通システムが求められているのです。
Views: 504